Vitamine C
LA VITAMINE C : UN CLASSIQUE EN NUTRITION
La vitamine C ou acide ascorbique est une vitamine intervenant dans les fonctions essentielles pour la santé de l’organisme. Cette vitamine hydrosoluble est considérée par les scientifiques comme l’un des plus grands antioxydants naturels.
Notre organisme ne sait pas produire et ni stocker cette vitamine, c’est pourquoi il est important de maintenir un apport quotidien. L'ANSES (agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail) conseille une dose quotidienne de 110mg de vitamine C par jour. L'ANSES a également fixé à 1000mg, la limite supérieure de sécurité. Cette limite comprend les apports alimentaires et les compléments alimentaires en vitamine C.
Bien que la vitamine C soit naturellement présente dans l’alimentation, la baisse de la qualité nutritionnelle des fruits et légumes rend intéressante la prise sous forme de compléments alimentaires.
Et pour en savoir plus, n'hésitez pas à lire notre guide sur la vitamine C.
- Contribue au fonctionnement normal du système immunitaire.
- Protège les cellules contre le stress oxydatif (antioxydant).
- Contribue au métabolisme énergétique et à réduire la fatigue.
- Favorise la synthèse du collagène.
- Contribue à des fonctions psychologiques et nerveuses normales.
- Aussi bien assimilée que la vitamine C contenue dans les fruits et légumes.

UNE VITAMINE QUI SE FAIT RARE DANS L'ALIMENTATION
L’acide ascorbique se trouve naturellement dans de nombreux fruits et légumes. Orange, kiwi, pamplemousse, cassis, poivrons rouge et vert, épinard, brocoli, choux de Bruxelles, fraises sont d’excellentes sources alimentaires en vitamine C.
Néanmoins, la culture intensive et le non-respect de la saisonnalité font que ces aliments apportent aujourd’hui moins de nutriments et de vitamines qu’il en faudrait malgré une alimentation équilibrée… C’est pourquoi une supplémentation en vitamine C permet de maintenir l’apport journalier nécessaire à l’organisme pour être en pleine santé.
D’après Philippe Desbrosses, Docteur en Sciences de l’environnement à l’université Paris-VII, il faudrait 100 pommes Golden du supermarché pour avaler autant de vitamine C (400 mg) qu’une pomme cultivée en 1950 !

Restez en bonne santé grâce à la vitamine C
L’apparition du scorbut chez les marins ayant une alimentation sans fruits et légumes pendant de longs mois a montré la nécessité de la vitamine C dans l’alimentation. Une carence en vitamine C peut se traduire par de nombreux symptômes.
En effet, la vitamine C contribue à :
- Réduire la fatigue et booster le métabolisme énergétique ;
- Assurer le fonctionnement normal du système immunitaire ;
- Maintenir le fonctionnement normal du système nerveux ;
- Assurer des fonctions psychologiques normales ;
- Protéger les cellules contre le stress oxydatif ;
- Accroître l’absorption de fer.
En particulier pour les sportifs, la vitamine C permet de synthétiser la carnitine. Elle joue un rôle majeur dans les contractions musculaires au cours des efforts longs et intenses. Elle permet également le transport des acides gras pour leur dégradation et leur transformation en énergie.
Enfin, la vitamine C a une influence sur le stockage du glycogène à partir de glycose, augmentant le stockage de ce dernier.

Une vitamine importante pour la synthèse du collagène
Le collagène est une protéine importante pour les tissus et l’élasticité de la peau. La vitamine C joue un rôle important pour maintenir un bon niveau de collagène dans l’organisme.
Des études ont montré que l’acide ascorbique contribue à la formation normale de collagène pour assurer le fonctionnement normal des vaisseaux sanguins, des os, des cartilages, des gencives, de la peau et des dents.
La présence du collagène dans le corps est capitale, surtout quand l’on est sportif : c’est grâce à cette protéine que vous restez mobile.
La synthèse du collagène déclinant avec l’âge, la prise d’un complément alimentaire de vitamine C permettra de maintenir un taux suffisant de vitamine C dans l’organisme.
Présentation générale
La vitamine C (ou acide ascorbique) est un composé organique hydrosoluble essentiel à l’organisme. Elle fût découverte pour la première fois au 18e siècle, lors d’un voyage maritime, où les matelots, qui ne consommaient que très peu de fruits et de légumes, furent touchés par une maladie très grave, le scorbut. Cette pathologie, qui donna son nom à l’acide ascorbique, est caractérisée par l’apparition de douleurs osseuses, de gingivorragie et une forte anémie. Un médecin de la marine anglaise, James Lind démontra l’efficacité de quelques gouttes de jus de citron ou d’orange dans le traitement préventif et curatif du scorbut. Cette maladie est en effet dû à une carence prolongée en vitamine C. En 1928, la vitamine C fût isolée du jus de citron, par le biochimiste hongrois, Albert Szent Györgyi qui reçut un prix Nobel pour sa découverte. Celle-ci intervient dans de nombreuses fonctions comme la défense contre les infections virales et bactériennes, la protection de la paroi des vaisseaux sanguins, l’assimilation du fer ou la cicatrisation.
La vitamine C n’est pas synthétisée ni stockée par l’organisme. C’est pourquoi il faut un apport alimentaire suffisant en cette dernière afin d’éviter les carences. Or, il s’agit de la vitamine la plus sensible, ainsi celle-ci est facilement dégradée par la chaleur, la lumière ou encore l’eau. Elle est ainsi très rapidement perdue dans l’alimentation, si les aliments sont cuits à trop forte température (au dela de 60°C, la vitamine est dégradée) ou bien exposés au soleil par exemple. (3) Il est ainsi conseillé de faire cuire les aliments riches en vitamine C à basse température ou à la vapeur si l’on veut conserver cette dernière. (36)
On retrouve cette vitamine dans tous les végétaux, cependant ce sont principalement les fruits et notamment les agrumes qui sont réputés pour leur forte teneur en vitamine C. (1) Ces derniers la synthétisent à partir du glucose ou du galactose. Aussi, la plupart des animaux contrairement aux Hommes peuvent synthétiser cette vitamine à partir du foie également à partir du glucose. (3)
Principales actions dans l’organisme
La vitamine C de formule brute C6H8O6 a la possibilité de s’impliquer dans de nombreuses réactions. En effet il s’agit d’un diacide, qui est un donneur d’hydrogène, et d’un réducteur. Il intervient ainsi dans de nombreuses réactions métaboliques dans l’organisme, qui expliquent ses nombreuses propriétés.
Réactions d’hydroxylations
(a) La synthèse du collagène : le collagène est la principale protéine permettant la constitution des fibres de collagène, participant à la formation mais aussi à la réparation des structures riches en tissu conjonctif comme les os, le cartilage, les ligaments ou les parois des vaisseaux sanguins.
En effet, l’acide ascorbique est un cofacteur permettant l’hydroxylation d’acides aminés, comme la proline qui s’hydroxyle en 4-hydroxyproline et de la lysine en 5-hydroxylysine, qui représentent jusqu’à 25% de la structure du collagène. (3)
(b) La synthèse des catécholamines : les catécholamines sont des neurotransmetteurs essentiels à l’activité du cerveau et au bon fonctionnement biologique. Ils sont représentés notamment par la dopamine, l’adrénaline et la noradrénaline. Ici, la vitamine C va participer à l’hydrolyse de la tyrosine, acide aminé essentiel à la synthèse des catécholamines. (3)
(c) La synthèse de la carnitine : la carnitine est une molécule jouant un rôle majeur dans la contraction musculaire au cours d’efforts longs et intenses. Au niveau des cellules musculaires, elle permet de transporter les acides gras au niveau des mitochondries afin que ces derniers soient dégradés dans le métabolisme énergétique. (5) En effet, cette synthèse nécessite une hydroxylation de la lysine, où la vitamine C joue un rôle de cofacteur enzymatique à deux fois.
Propriétés antioxydantes
Les cellules de notre corps doivent faire face à un stress oxydatif par de nombreux mécanismes. La vitamine C fait partie des quatre antioxydants les plus souvent retrouvés dans l’alimentation avec la vitamine E, le bêtacarotène et le sélénium. (2) Un antioxydant est défini comme « une substance qui, à faible concentration par rapport à son substrat oxydable (par exemple les protéines, les lipides, les acides nucléiques), prévient ou réduit l’oxydation de ce substrat ». (6)
(a) Lutte contre le stress oxydatif : la vitamine C est donc capable d’éliminer les espèces réactives de l’oxygène et de l’azote telles que les radicaux superoxyde et hydroperoxyle, l’oxygène singulet, l’ozone, le peroxynitrite, les radicaux nitroxyde, l’acide hypochloreux ou le dioxyde d’azote. Ce sont des molécules instables auxquelles il manque un électron, qui vont essayer d’arracher ce dernier aux constituants cellulaires. Des excès de tels produits sont associés à l’oxydation de composés essentiels comme l’ADN, les protéines ou les lipides. (4)
L’acide ascorbique est un réducteur très puissant, ce qui lui confère son pouvoir antioxydant. On peut ainsi le retrouver sous trois degrés d’oxydoréduction différents (7) :
La forme réduite correspond à l’acide ascorbique, retrouvée dans la nature et l’alimentation et qui possède le pouvoir anti-oxydant recherché. Il y a également une forme mono-oxydée, appelée acide mono-déhydro-ascorbique et enfin la forme oxydée ou acide déhydro-ascorbique. La forme intermédiaire est un radical anion inerte et peu réactif, qui est un intermédiaire entre la forme oxydée et réduite. Ainsi, via sa forme réduite, l’acide ascorbique va prendre en charge les composés réactifs générant du stress oxydatif en leur fournissant un électron, ce qui va les rendre inertes et non toxiques. (4)
(b) Réduction de la méthémoglobine et hémoglobine : l’atome de fer retrouvé au niveau de l’hémoglobine (Fe2+) est exposé en permanence à de fortes concentrations d’oxygène qui l’oxydent au cours du temps. Lorsque le fer de l’hémoglobine s’oxyde, l’érythrocyte devient alors incapable de transporter l’oxygène car l’hémoglobine se transforme en méthémoglobine (avec un atome de fer Fe3+), incapable de fixer l’O2. (10) Un taux trop élevé de méthémoglobine peut causer une méthémoglobinémie, très dangereuse pouvant entrainer des troubles respiratoires et une hypoxie des organes (8).
L’acide ascorbique étant un puissant anti-oxydant, il permet de participer au ralentissement de cette oxydation de l’hémoglobine afin de conserver un taux minimal de méthémoglobine dans le sang circulant et de conserver une bonne oxygénation des organes.
Inhibition de la formation des nitrosamines
On appelle nitrosamines, ou N-nitrosamines, les molécules qui contiennent le groupement fonctionnel N-nitroso. Ces substances font partie de la « cohorte préoccupante », un groupe de substances mutagènes que le Centre international de Recherche sur le Cancer de l’Organisation mondiale de la Santé a classé comme probablement cancérogènes pour l’homme. (11) Les nitrosamines se forment à partir des nitrites alimentaires retrouvées dans certains aliments (viande fumée, légumes macérés au vinaigre par exemple) ou produits par certaines bactéries. La vitamine C a la capacité d’inhiber cette transformation qui se fait au niveau de l’estomac, à pH acide. (14)
Figure 6 : formation des nitrosamines à partir des nitrites
Au niveau de l’estomac, le pH acide est favorable à a la réaction d’oxydation de l’acide ascorbique en acide déhydro-ascorbique. Une fois formé, l’acide déhydro-ascorbique réagit avec les nitrites en empêchant leur transformation en composés N-nitrosés. (13)
La supplémentation en vitamine C
La supplémentation en vitamine C peut s’avérer essentielle. N’étant pas synthétisée par l’organisme, il est très rapidement possible de se retrouver carencé en vitamine C si celle-ci n’est pas suffisamment apportée par l’alimentation. Également, sa fragilité fait que si les aliments ne sont pas correctement stockés ou cuisinés, ils perdront une grande partie de leur teneur en acide ascorbique.
Aspect règlementaire
La directive européenne 2002/46/CE limite la notion de nutriments aux seuls vitamines et minéraux. Elle établit dans son annexe I une liste exhaustive de 13 vitamines et de 17 minéraux qui peuvent être utilisés dans la fabrication des compléments alimentaires. L’annexe II de cette directive précise les formes d’apport qui peuvent être employées. La vitamine C figure parmi les 13 autorisées et est autorisée sous 7 formes différentes (acide L-ascorbique utilisé ici y compris).
Les recommandations sanitaires pour ce qui concerne la teneur maximale recommandée en vitamine C dans les compléments alimentaires sont de 1000 mg par jour selon la Direction Générale de la concurrence, de la consommation et de la répression des fraudes. (39)
Aspect pharmacocinétique
Absorption = l’absorption de la vitamine C prise par voie orale se fait principalement au niveau digestif, plus précisément au niveau du duodénum et du jéjunum proximal, donc les parties hautes de l’intestin. Cette absorption est saturable et le pourcentage absorbé diminue avec la dose. Par exemple :
- après une prise de 200 mg, 100% de la dose est absorbée soit 200 mg. C’est la dose pour laquelle la biodisponibilité est maximale. (37) C’est la dose d’acide ascorbique retrouvée dans le multivitamines de Nutripure ® (42)
- après une prise de 1g, 75% de la dose est absorbée (soit 750mg).
- après une prise de 5g, seulement 20% est absorbé (soit 1g).
Figure 7 : impact du dosage en vitamine C par voir orale sur le taux de concentration plasmatique
Cette absorption est rapide et dépend des transporteurs actifs sodium-dépendants de l’intestin. (20)
Distribution = les proportions relatives d’acide ascorbique et d’acide déhydro-ascorbique sont de 90% et 10% dans l’organisme. La forme réduite prédomine parce qu’elle est protégée par le glutathion et les composés à groupe SH. Dans le plasma, l’acide ascorbique est lié réversiblement à l’albumine. La concentration plasmatique considérée comme normale chez l’adulte est supérieure à 6 mg/L, les valeurs inférieures que l’on rencontre fréquemment chez les personnes âgées traduisent une déficience.
Les leucocytes sont riches en vitamine C, ils en contiennent 80 fois plus que le plasma. Les tissus les plus riches en vitamine C sont le cortex surrénal et l’hypophyse et, à moindre degré, le foie, le muscle et la cornée. Il n’y a pas de véritable forme de stockage de la vitamine C et, lorsque l’apport cesse, les réserves chutent en deux à trois semaines, la demi-vie corporelle de la vitamine C étant de dix à vingt jours. (20)
Métabolisme = l’acide ascorbique est facilement oxydé en acide déhydro-ascorbique. Après dégradation irréversible, l’acide 2,3-dicétogulonique (produit de dégradation sans action biologique) est ensuite oxydé en acide oxalique et acide thréonique.
Elimination = la voie principale d’excrétion de l’acide ascorbique est la voie urinaire mais un petit pourcentage est excrété dans les fèces. Les doses excédantes qui sont absorbées sont majoritairement excrétées sous forme inchangée dans les urines. Chez l’Homme, la demi-vie plasmatique de l’acide ascorbique est de 16 jours. (19)
Aspect pharmacodynamique
Classe pharmacothérapeutique : acide ascorbique (vitamine C), code ATC : A11GA01.
La vitamine C est essentielle à l’Homme. Ses composants, l’acide ascorbique et l’acide déshydroascorbique, forment un important système redox.
En tant qu’antioxydant et cofacteur enzymatique, l’acide ascorbique a une fonction spéciale dans cette interaction redox et joue un rôle crucial dans différentes réactions d’hydroxylation. Il existe plusieurs mono- et di-oxygénations ascorbate-dépendantes dans différents processus de synthèse d’hormones et de neurotransmetteurs. L’ascorbate de sodium est également requis pour l’hydroxylation de la carnitine.
Il a été avancé qu’un déficit en carnitine pouvait être responsable des premiers symptômes du scorbut. La vitamine C a certaines fonctions biologiques qui peuvent influencer la production d’énergie et donc les performances physiques.
En plus de son rôle dans la synthèse du collagène et de la carnitine, du fait du transport d’acides gras à longue chaîne dans la mitochondrie, la vitamine C est également nécessaire pour la synthèse des catécholamines, de l’épinéphrine et de la norépinéphrine.
L’acide ascorbique facilite le transport et l’absorption par la muqueuse du fer non-héminique, la réduction des intermédiaires de l’acide folique et la synthèse du cortisol. La vitamine C est un puissant antioxydant qui sert à régénérer la vitamine E à partir de ses composés oxydés. (19)
Les dangers d’une carence en vitamine C
Origines des carences vitaminiques
On distingue plusieurs origines aux carences vitaminiques. Cela peut être dû à un défaut d’absorption, d’apport ou bien à des besoins majorés chez certaines personnes.
(a) Carences d’absorption : comme elles ne sont apportées qu’essentiellement via l’alimentation, une mauvaise absorption peut rapidement conduire à un déficit vitaminique. Les cas les plus courants sont des perturbations du transit digestif, qui serait accéléré et diminuerait le temps de transit intestinal, ou une inhibition de leur absorption par un autre médicament. Par exemple dans le cas de la vitamine C, l’absorption est réduite en cas de prise d’aspirine à fortes doses.
(b) Carences par besoins majorés : certaines circonstances, physiologiques ou pathologiques, nécessitent un apport de vitamines plus conséquent que la normale en raison de besoins accrus ou augmentés de l’organisme pour diverses raisons. Par exemple, les femmes enceintes, les alcooliques, les personnes touchées par certaines maladies infectieuses, peuvent nécessiter une supplémentation en vitamines afin de répondre à leurs besoins. Également, lors du traitement au long cours par certains médicaments comme l’iso-niazide, la metformine, les contraceptifs oraux ou les sulfamides, les besoins vitaminiques sont perturbés et une prise en charge doit être mise en place afin de prévenir les déficits occasionnés.
(c) Carences d’apport : la plus courante, qui est occasionnée par une alimentation mal équilibrée ou insuffisante, qui n’apporte pas la quantité nécessaire de vitamines à l’organisme. Elle est fréquente chez les personnes âgées en raison de pertes d’appétit. (20)
Conséquences d’une carence en vitamine C
Une carence en vitamine C peut avoir de très lourdes conséquences. En effet cette dernière participe à de nombreux mécanismes, ainsi un manque de celle-ci peut occasionner des symptômes divers, et dans les cas extrêmes elle est responsable d’une pathologie : le scorbut.
Une carence discrète se traduit par divers symptômes, découlant directement des propriétés de cette vitamine : asthénie, perte d’appétit, amaigrissement, céphalées, douleurs osseuses, moindre résistance aux infections et troubles hémorragiques (20). La tranche d’âge la plus concernée par ces carences discrètes sont les personnes de plus de 65 ans. (2)
Une carence sévère se manifeste par le scorbut, qui est beaucoup plus dangereux : il se caractérise notamment par un syndrome hémorragique grave, des troubles de la cicatrisation, des œdèmes, des signes rhumatismaux ou encore des atteinte gingivales. L’évolution peut être létale en l’absence d’apport en vitamine C. Le diagnostic d’une carence peut être effectué par un dosage de la vitamine C dans le plasma sanguin. La concentration normale est de l’ordre de 10mg/L. (22)
Contre-indications et effets indésirables
Même à fortes doses, la vitamine C est une molécule qui a peu d’effets indésirables.
Pour une dose supérieure à 1g/j : il est possible de rencontrer des troubles digestifs (brûlures d’estomac, diarrhées, douleurs abdominales), des céphalées, des difficultés d’endormissement et agitation (étant un excitant, il est conseillé de prendre la vitamine C le matin) ainsi que des troubles urinaires (gêne à la miction, coloration légère des urines).
Pour une dose supérieure à 3g/j : une hémolyse des globules rouges est possible chez les personnes déficientes en G6PD, engendrant une anémie et fatigue. (19)
L’hypersensibilité à la vitamine C est très rare. Également, l’hypervitaminose C n’existe pas, du fait de l’élimination des excès directement dans les urines et les selles. (2)
En ce qui concerne les contre-indications, elles sont également peu nombreuses mais certaines situations déconseillent la supplémentation en vitamine C :
Les personnes sujettes aux lithiases rénales oxalo-calciques (troubles du métabolisme du fer, déficit en G6PD) : les calculs des voies urinaires sont une contre-indication à la prise de vitamine C à des doses supérieures à 1g/j. En effet, l’oxalate est l’un des produits du métabolisme de cette dernière et peut s’accumuler dans les urines et engendrer des calculs rénaux.
Les personnes en surcharge de fer : la vitamine C favorise l’assimilation du fer libre en en transformant le fer ferrique en fer ferreux, mieux absorbé. Ainsi en cas de surcharge préexistante, cela va amplifier cette dernière et éventuellement déclencher des manifestations toxiques.
Avant un test biologique : la prise de vitamine C est déconseillée avant les dosages sanguins, urinaires et la mesure de la créatinine à une dose supérieure à 2g/j. En effet, il est possible qu’elle interfère et fausse les résultats de ces tests, elle est donc à éviter. (2)
Allégations scientifiques disponibles pour la vitamine C et leurs justifications scientifiques
La vitamine C a de nombreuses vertus et sont utilisation est très variée. Cependant, il est nécessaire de justifier ces allégations par des études cliniques et toxicologies et de se baser sur des travaux existants confirmant ces indications. Ici, trois allégations sont portées sur la vitamine C :
- La vitamine C réduit le stress oxydatif et protège les cellules de notre organisme ;
- La vitamine C contribue au fonctionnement normal du système immunitaire ;
- La vitamine C participe au fonctionnement du métabolisme énergétique et réduit la fatigue.
Intérêt de la vitamine C sur le stress oxydatif
Données disponibles
Les propriétés antioxydantes de la vitamine C sont étudiées depuis de nombreuses années. Son mécanisme d’action est déjà bien connu (1.2.2.a), et explique sur le plan physico-chimique le potentiel antioxydant de cette molécule. Cependant, des études in vivo sur des volontaires ont été menées afin de confirmer cette action dans l’organisme et son réel bénéfice.
Une étude a été menée en 2002 (24) pour démontrer l’effet antioxydant de la vitamine C sur l’organisme chez des patients intoxiqués au paraquat, un herbicide et puissant poison engendrant une grande toxicité sur les cellules via notamment la création de radicaux libres. L’étude du statut antioxydant total (TAS) a été retenue, en effet celui-ci reflète la capacité globale de l’organisme à se défendre contre les radicaux libres et permet une bonne estimation du niveau d’équilibre pro-oxydant/antioxydant.
Cette étude consistait en 4 modèles expérimentaux.
- Dans un premier temps, les valeurs de base du TAS et de vitamine C ont été évalués chez 56 adultes en bonne santé : cette expérience a été menée à titre de recherche préliminaire. Les moyennes de TAS et de vitamine C mesurées chez les 56 volontaires sains étaient respectivement de 2,22 ± 0,16 mmol-1 et 0,48 ± 0,10 mg / dl. Des corrélations positives entre la vitamine C et la TAS ont été observées, c’est-à-dire que plus le taux de vitamine C était élevé, plus le TAS augmentait.
Figure 8 : Nuages de points et corrélation entre la vitamine C et le TAS in vivo
- Dans un second temps, la relation in vitro entre la vitamine C et le TAS a été évaluée : diverses concentrations de vitamine C ont été administrées juste avant la mesure du TAS sur un plasma humain in vitro. On remarque la même chose que dans l’expérience in vivo, avec une corrélation positive entre les taux de vitamine C et les valeurs de TAS. Cette corrélation est plus marquée que dans l’expérience in vivo.
Figure 9 : Nuages de points et corrélation entre la vitamine C et le TAS in vitro
- Dans un troisième temps, une étude pharmacocinétique de la vitamine C a été menée in vivo chez 7 volontaires sains en évaluant le TAS après l’administration de vitamine C : après injection de vitamine C dans le sang, plusieurs mesures du TAC et du taux de vitamine C ont été effectuées pour obtenir des données pharmacocinétiques. Les niveaux de vitamine C dans le plasma ont culminé en 30 minutes avec une variation interindividuelle, puis ont diminué lentement.
Figure 10 : évolution temporelle de la vitamine C plasmatique pour la pharmacocinétique chez sept volontaires après injection de 3000 mg de vitamine C
Les résultats pharmacocinétiques de la vitamine C étaient les suivants: volume de distribution = 32,0 ± 14,4 l, AUC (aire sous la courbe) = 36,4 ± 11,3 mg h / dl, clairance plasmatique = 2,13 ± 1,36 l / h, demi-vie ( T 1/2 ) = 1,0 ± 0,8 h, C max (concentration maximale) = 17,1 ± 7,1 mg / dl et T max (temps de concentration maximale) = 0,64 ± 0,24 h. - Dans un dernier temps, une évaluation de la relation entre l’administration de vitamine C et une modification du TAS a été faite chez 10 patients intoxiqués au paraquat : des quantités croissantes de vitamine C ont été administrées pendant 5 jours consécutifs chez des patients intoxiqués au paraquat. Des échantillons de sang ont ensuite été prélevés 1h après chaque administration pour mesurer le TAS.
Comme les quantités de vitamine C ont augmenté pendant 5 jours consécutifs chez 10 patients intoxiqués au paraquat, le TAS a été augmenté comme suit:
o J1 (100 mg de vitamine C) TAS = 2,26 ± 0,98 mmol-1
o J2 (500 mg de vitamine C) TAS = 2,76 ± 0,78 mmol-1
o J3 (1000 mg de vitamine C) TAS = 2,81 ± 0,68 mmol-1
o J4 (3000 mg de vitamine C) TAS = 3,18 mmol-1
o J5 : 3000 mg de vitamine C ont été administrés en bolus intraveineux trois fois (toutes les 8 h pendant un jour), le TAS après la dernière dose était = 3,58 ± 0,37 mmol-1.
Conclusion
Cette étude a donc permis de montrer un lien entre l’administration de vitamine C et une augmentation du statut antioxydant total de l’organisme. Les résultats entre l’étude in vivo et in vitro de cette corrélation sont cohérents et la variation relative du test n’a pas dépassé les 10%. Chez les patients, aucun effet secondaire n’a été observé même à la dose maximale de 3000 mg.
La vitamine C est donc un antioxydant utile et efficace chez l'homme; ainsi, la vitamine C peut être utilisée comme piégeur de radicaux libres au stade aigu de la peroxydation lipidique par le paraquat, et son effet protecteur sur les cellules en piégeant les radicaux libres (1.2.2.a) dans l’organisme est avéré.
Intérêt de la vitamine C sur le système immunitaire
Données disponibles
De nombreuses études ont été menées concernant le rôle de la vitamine C sur le système immunitaire. Certains phénomènes restent mal compris en ce qui concerne son mécanisme d’action sur les cellules de l’immunité, cependant des études cliniques in vivo et in vitro ont permis de démontrer de véritables propriétés à ce niveau.
(a) L’une des premières expériences à ce sujet fut menée par Goetzl EJ et al. en 1974. (28) Ils ont démontré que lors de l'incubation de leucocytes humains avec de l'acide ascorbique à pH neutre et à des concentrations 10 à 50 fois supérieures à celles des taux sanguins normaux, la migration aléatoire in vitro et la chimiotaxie des cellules augmentait de 100 à 300% sans influencer leur capacité phagocytaire. La chimiotaxie définit la migration des neutrophiles en extravasculaire vers les sites infectés pour exercer leur fonction d’immunité. Ils répondent à différents signaux, notamment la sécrétion de substances pro-inflammatoires comme l’interleukine 8 (Il-8), le leucotriène B4 ou les protéines du système du complément. (16) En augmentant ce dernier, cela favorise la migration des neutrophiles au niveau du site infectieux. (15)
(b) En parallèle, en 1973, une étude menée par Hume R. (30) L'acide ascorbique leucocytaire a été mesuré chez 7 sujets pendant le rhume. Il y a eu une chute significative du taux de vitamine C aux niveaux scorbutiques dans les 24 heures suivant l'apparition des symptômes. Au cinquième jour, cette valeur était revenue à la normale, ce qui coïncidait avec la cessation des symptômes. Ainsi il a été suggéré une utilisation de la vitamine C par les leucocytes pour lutter contre le rhume.
À la suite de ces découvertes, la science s’est de plus en plus intéressée à ces phénomènes liant la vitamine C au système immunitaire et d’autres études ont été menées.
(c) Des études de l’EFSA ont également montré qu’un apport de vitamine C (entre 200 mg et 6 g par jour) modifiait certains marqueurs de la réponse immunitaire : activité des cellules Natural Killer, prolifération de lymphocytes et production de cytokines pro-inflammatoires (26)
(d) Une étude de 2013 fut engagée par Karger AG et al. (31) 33 volontaires ont été supplémentés par de la vitamine C ou un placebo pendant 4 semaines. L'activité de piégeage des radicaux cutanés a 14 CONFIDENTIEL été mesurée par spectroscopie par résonance paramagnétique électronique. Après 4 semaines, l'apport de 100 mg de vitamine C/jour a entraîné une augmentation significative de l'activité de piégeage des radicaux de 22%. La prise de 180 mg/jour a même entraîné une augmentation significative de 37%. Aucun changement n'a été trouvé dans le groupe placebo. Une partie de la population étudiée a également été mesurée après 2 semaines: dans ce groupe, le piégeage des radicaux avait déjà atteint une activité maximale après 2 semaines. En conclusion, la vitamine C administrée par voie orale augmente l'activité de piégeage des radicaux de la peau. L'effet se produit rapidement et est amélioré avec des doses plus élevées de vitamine C.
La barrière naturelle que constitue la peau a pour fonction principal la protection de l’organisme vis-à-vis des agents extérieurs, notamment pathogènes. En effet la rupture de cette barrière est propice à l’entrée des micro-organismes dans notre corps et aux infections. (38) Du fait de son rôle dans la synthèse du collagène (1.2.1.a), la vitamine C permet de préserver cette barrière et sa reconstruction en cas de rupture de cette dernière en aidant à la cicatrisation. Également, grâce à ses propriétés antioxydantes (1.2.2.a), elle préserve les membranes cellulaires de l’oxydation, ces dernières étant essentiellement constituées de lipides et de protéines.
Conclusions
La vitamine C soutient différents aspects du système immunitaire inné et adaptatif, y compris la fonction de barrière épithéliale, la chimiotaxie, les activités antimicrobiennes des cellules phagocytaires, les fonctions des lymphocytes NKT ainsi que la prolifération et différenciation des lymphocytes. (15) Malgré le fait que les mécanismes soient encore mal connus, il a été démontré une réelle efficacité in vitro et in vivo de l’administration de vitamine C dans le support des fonctions du système immunitaire.
Intérêt de la vitamine C sur le métabolisme énergétique et la fatigue
Données disponibles
(a) Vitamine C et métabolisme : cette allégation repose principalement sur une propriété de la vitamine C qui permet le stockage du glycogène dans les muscles et le foie. Le glycogène est un glucide complexe polymère du glucose. Il constitue une réserve d’énergie chimique qui permet de libérer rapidement du glucose pour le transformer en énergie lors d’un effort physique. Lors d’une activité sportive, l’organisme peut utiliser plusieurs sources d’énergie (glucose, lipides, acides aminées…) dans des proportions variables selon l’intensité et la durée de l’effort. Cependant lorsque ce dernier est intense, le glucose est le nutriment utilisé en priorité par les muscles. Il est également la seule source d’énergie utilisable par le cerveau et le système nerveux. Cette réserve de glycogène est donc essentielle pour ne pas tomber en épuisement physique lors d’un effort sportif prolongé. Pour apporter du glucose en quantité suffisante aux muscles, l’organisme dégrade le glycogène musculaire. Un épuisement de ces réserves se traduira par une fatigue importante qui limitera les performances sportives.
Une étude a été effectuée par Ratsimamanga, A. afin d’évaluer l’influence de l’acide ascorbique sur le comportement de l’organisme, notamment en observant l’évolution du glycogène. Elle est menée sur des cobayes murins, qui synthétisent eux même la vitamine C contrairement à l’Homme. Certains cobayes ont volontairement été placés en carence vitaminique et les variations en glycogène dans les différents tissus ont été mesurées.
Figure 11 : Evolution du glycogène au cours de la carence C ou scorbut expérimental chez le cobaye
Il a ensuite été mis en parallèle les taux de glucides chez le cobaye carencé et non carencé afin de faire une comparaison entre des individus carencés en vitamine C et des individus ou l’apport était suffisant.
Figure 12 : comparaison entre l'animal normal et l'animal complètement carencé
Enfin, les cobayes ont été supplémentés avec différentes doses d’acide ascorbique afin d’observer si le glycogène remontait lors de cette opération. Les doses ont été augmentées sur plusieurs jours en mesurant à chaque fois le taux de glycogène hépatique.
Figure 13 : évolution du glycogène hépatique en fonction de l'acide ascorbique
Cette étude a donc permis de mettre en lumière le lien entre la vitamine C et le métabolisme énergétique. En effet, plus l’organisme en reçoit des doses élevées, plus le glycogène ainsi que d’autres substances impliquées dans la contraction musculaire comme l’acide créatine-phosphorique augmentent et inversement en cas de carence. Ces faits ont des répercussions dans la physiologie du travail musculaire de tous les organismes, et spécialement chez ceux qui ne synthétisent pas la vitamine C, comme l’Homme.
(b) Vitamine C et fatigue : c’est une allégation très courante concernant a vitamine C, pour laquelle de nombreuses personnes souhaitent une supplémentation . (34) Une étude fut menée par Corey J. Huck et al. en 2013 (33) sur des adultes obèses adhérant à un régime hypocalorique. Leur perception de l’effort et leur niveau de fatigue après un effort avec et sans supplémentation en vitamine C ont été évalués. Cette étude incluait 20 patients recevant au hasard 500 mg de vitamine C ou un placebo par jour pendant 4 semaines.
Figure 14 : Scores de fatigue et changements de performance après 60 min de marche au départ puis a la semaine 4 de l'étude pour les groupe CV (avec vitamine C) et CON (placebo)
Après ces 4 semaines, les deux groupes ont perdu des quantités similaires de poids (~ 4 kg), et le rapport d'échange respiratoire n'a pas été modifié par groupe. La fréquence cardiaque et les évaluations de l'effort perçu pendant l'exercice ont été significativement diminuées dans le groupe recevant la vitamine C par rapport au groupe placebo. Quant au score de fatigue générale, il a été diminué de 5,9 U pour le groupe recevant la vitamine C par rapport à une augmentation de 1,9 U pour le groupe placebo. Ces données fournissent des preuves préliminaires que le statut en vitamine C peut influencer la fatigue, la fréquence cardiaque et la perception de l'effort pendant un exercice modéré chez les personnes obèses.
Conclusions
En plus d’améliorer l’absorption du fer, ce qui permet aux globules rouges de transporter l’oxygène dans tout le corps, la vitamine C contribue au métabolisme énergétique normal et à la réduction de la fatigue et de l’épuisement. (32). En favorisant le stockage du glycogène, elle permet de réduire le glucose sanguin et d’établir des réserves énergétiques pour les efforts au long cours.
Également, il a été démontré une baisse de la fatigue générale significative chez les personnes supplémentées en vitamine C par rapport a un groupe placebo après un effort physique. (34)
Autres intérêts de la vitamine C
Impact sur l’absorption du fer
Il existe 2 formes différentes de fer : le fer héminique et le fer non héminique. Le fer non héminique se trouve majoritairement dans les produits laitiers et les végétaux. Il est présent sous la forme de fer ferrique Fe 3+ et a une biodisponibilité équivalente à 2 à 20 %. Le fer héminique est retrouvé au sein des globules rouges et est retrouvé dans les viandes, poissons et crustacés. Sa biodisponibilité est d’environ 15 à 25%, ainsi il est mieux absorbé. La vitamine C jouerait un rôle dans l’absorption du fer non héminique du fait de son potentiel réducteur, en transformant le Fe3+ en fer ferreux Fe2+. Ce fer ferreux est beaucoup mieux absorbé par le corps. (39)
Une étude a été menée par James D. Cook et al. (40) Elle a permis d’étudier l’absorption concomitante de vitamine C et de fer pour observer la relation entre les deux composés. Les tests d’absorption ont été faits sur 63 volontaires sains âgés de 18 à 32 ans. 2 tests ont été réalisés sur chaque sujet, un après un repas et un après un repas + vitamine C à différentes doses. C’est l’absorption du fer non héminique qui a été observée ici.
- Le premier groupe de 12 sujets a reçu le repas sans acide ascorbique et avec 25, 50 et 100 mg. L’absorption moyenne géométrique de ces repas était de 0,77, 1,27, 1,94 et 3,19%, respectivement.
- Le deuxième groupe de 13 sujets a reçu le 55 repas sans vitamine C et avec 250, 500 et 1, 000 mg. L'absorption moyenne de ces repas était de 0,74, 3,48, 4,59 et 7,10%, respectivement (figure 15).
L'effet des variations d'absorption du fer entre les sujets en raison de différences du statut en fer peut être éliminé en calculant pour chaque sujet le rapport entre l'absorption du fer avec de l'acide ascorbique et l'absorption du fer sans acide ascorbique. Avec la dose la plus faible de 25 mg, ce rapport était en moyenne de 1,65, ce qui représentait une augmentation significative de l'absorption du fer (t = 2,71, P <0,01). Plus grandes les quantités d'acide ascorbique étaient, plus ont observait une augmentation de ce rapport d'absorption: 2,53 avec 50 mg, 4,15 avec 100 mg, 4,70 avec 250 mg, 6,19 avec 500 mg et 9,57 avec 1 000 mg. La relation entre le quantité d'acide ascorbique ajoutée et l'augmentation de l'absorption du fer était linéaire sur une échelle logarithmique (figure 16).
Figure 15 : effets de l'acide ascorbique sur l'absorption du fer après repas
Figure 16 : relation entre la quantité d'acide ascorbique administré et l'absorption du fer non héminique
Cette étude a donc permis de montrer la corrélation positive entre l’administration de vitamine C et l’absorption du fer. Plus la quantité de vitamine C administrée avec un repas est élevée, plus le fer non héminique absorbé est élevé. Or, ce dernier est essentiel à l’organisme en participant aux réserves et transport du fer, ainsi qu’au fonctionnement de diverses enzymes. (40)
Impact sur le cholestérol
Une autre allégation concerne la capacité de la vitamine C à intervenir sur la réduction du cholestérol. Une revue et analyse de 51 essais expérimentaux a été effectuée par Marc P. McRae et al. en 2006. (41) Face à des résultats parfois incohérents entre différentes études menées chez l’Homme, une recherche de Medline a été effectuée sur des études de 1996 à 2004, regroupant 1666 sujets au total.
Les études ont été séparées en 4 groupes selon le taux de cholestérol de base des sujets observés : sévère, très haut, haut et normal. Il a été observé que chez les personnes avec un haut taux de cholestérol de base, le changement moyen observé avec une supplémentation en vitamine C a été le plus spectaculaire.
Figure 17 : changements observés en fonction du taux de cholestérol de base chez différents patients supplémentés en vitamine C
Pour les populations hypercholestérolémiques sévères (> 280 mg / dl), la vitamine C est capable d'obtenir des diminutions comparables du cholestérol sérique total par rapport à d'autres compléments nutritionnels comme la niacine (vitamine B3), et contrairement à cette dernière la vitamine C comporte très peu d’effets indésirables. Une corrélation à été observée entre le taux de base du cholestérol des patients et la diminution de ce dernier après l’administration de vitamine C.
Figure 18 : changement du cholestérol dans le sérum total après une supplémentation en vitamine C en fonction du taux de cholestérol de base
Le taux de cholestérol sérique total au départ peut prédire la mortalité cardiovasculaire à long terme. Par conséquent, une supplémentation quotidienne d'un minimum de 400 mg de vitamine C pour les patients ayant des taux de cholestérol sérique total supérieurs à 240 mg / dl peut avoir bienfaits pour la santé. Le bénéfice semble être le plus prononcé chez les patients atteints d'hypercholestérolémie sévère (cholestérol sérique total supérieur à 280 mg / dl) qui, en parallèle, sont bien souvent en carence de vitamine C avec des valeurs plasmatiques inférieures à 0,6 mg / dl.
Par conséquent, d'autres essais randomisés, en double aveugle et contrôlés par placebo sont nécessaires pour soutenir l'efficacité de la supplémentation en vitamine C chez les patients hypercholestérolémiques de haut à sévère.
Conclusion
La vitamine C est donc une vitamine essentielle pour l’organisme. Du fait de ses propriétés physico-chimiques, cette molécule acide et réductrice est impliquée dans de nombreuses réaction et a des rôles très importants dans le métabolisme énergétique, l’immunité et le piégeage des radicaux libres qui abîment nos cellules. N’étant pas synthétisée par l’homme, son apport via l’alimentation est essentiel. Cependant, étant une vitamine très fragile, il peut arriver que cet apport alimentaire soit insuffisant et doive faire l’objet d’une supplémentation.
Bibliographie
(1) ANSES. 2019. Vitamine C ou acide ascorbique.
(2) Jacques Buxeraud, Sébastien Faure. 2021. La vitamine C, Actualités Pharmaceutiques, Volume 60, Issue 604. S24-S26.
(3) Paul M Dewick. 2002. Medicinal Natural Products, A Biosynthetic Approach, Second Edition. 409- 472.
(4) Johnston, C.S., Steinberg, Francene, Rucker, Robert. 2013. Ascorbic Acid. Handbook of Vitamins. 489-520. 10.1201/b15413-15.
(5) J.D. Hulse, S.R. Ellis, L.M. Henderson. Carnitine biosynthesis 1978. beta-Hydroxylation of trimethyllysine by an alpha-ketoglutarate-dependent mitochondrial dioxygenase. Journal of Biological Chemistry, Volume 253. 1654-1659.
(6) Food and Nutrition Board. 1998. Dietary Reference Intakes. National Academy Press, Washington, DC.
(7) Beyer, R.E. 1994. The role of ascorbate in antioxidant protection of biomembranes: Interaction with vitamin E and coenzyme Q. J Bioenerg Biomembr 26, 349–358.
(8) Organisation Mondiale de la Santé. 2021. Les maladies liées à l’eau, méthémoglobinémie.
(9) Dötsch, J., Demirakça, S., Cryer, A. et al. 1998. Reduction of NO-induced methemoglobinemia requires extremely high doses of ascorbic acid in vitro. Intensive Care Med 24, 612–615.
(10) Mansouri A, Lurie AA. 1993. Concise review: methemoglobinemia. Am J Hematol ;42(1):7-12
(11) Organisation Mondiale de la Santé. 2021. Mise à jour sur les impuretés de nitrosamines.
(12) Tannenbaum SR, Wishnok JS, Leaf CD. 1991. Inhibition of nitrosamine formation by ascorbic acid. Am J Clin Nutr ;53(1 Suppl):247S-250S.
(13) Tannenbaum SR. 1989. Preventive action of vitamin C on nitrosamine formation. Int J Vitam Nutr Res Suppl ; 30:109-13. PMID: 2507690.
(14) Mirvish SS, Wallcave L, Eagen M, Shubik P. 1972. Ascorbate-nitrite reaction: possible means of blocking the formation of carcinogenic N-nitroso compounds. Science ;177(4043):65-8.
(15) Carr AC, Maggini S. 2017. Vitamin C and Immune Function. Nutrients ; 9(11):1211
(16) Chollet-Martin S. 2007. Chimiotactisme des polynucléaires neutrophiles, service d'hématologie et d'immunologie biologiques, hôpital Bichat.
(17) Amber Parker, Sarah L. Cuddihy, Tae G. Son, Margreet C.M. Vissers, Christine C. Winterbourn. 2011. Roles of superoxide and myeloperoxidase in ascorbate oxidation in stimulated neutrophils and H2O2-treated HL60 cells, Free Radical Biology and Medicine,Volume 51, Issue 7, 1399-1405,
(18) Légifrance. 2006. Arrêté du 9 mai 2006 relatif aux nutriments pouvant être employés dans la fabrication des compléments alimentaires.
(19) Base de données publiques des médicaments. 2019. Vitamine C Arrow, résumé des caractéristiques du produit.
(20) Pierre Allain. Pharmacologie, les Médicaments, Troisième édition. 2000. 459-45222 CONFIDENTIEL
(21) Jean-Louis Schlienger. 2020. Le scorbut : d’hier à aujourd’hui, Médecine des Maladies Métaboliques, Volume 14, Issue 1, Pages 69-76
(22) Haute autorité de santé. 2018. Doser la vitamine C chez un patient n’est éventuellement utile que pour confirmer un scorbut.
(23) Dragsted, L.O. 2008. Biomarkers of exposure to vitamins A, C, and E and their relation to lipid and protein oxidation markers. Eur J Nutr 47, 3.
(24) B Frei, L England, B N Ames. 1989. Ascorbate is an outstanding antioxidant in human blood plasma, Proceedings of the National Academy of Sciences, 86 (16) 6377-6381
(25) Sae-Yong Hong, Kyu-Yoon Hwang, Eun-Young Lee, Soo-Whon Eun, Suk-Ran Cho, Chan-Soo Han, Yung-Hyun Park, Sung-Keun Chang. 2002. Effect of vitamin C on plasma total antioxidant status in patients with paraquat intoxication, Toxicology Letters,Volume 126, Issue 1, Pages 51-59.
(26) Mónica De la Fuente, Carmen Sánchez, Carmen Vallejo, Estefanía Díaz-Del Cerro, Francisco Arnalich, Ángel Hernanz. 2020. Vitamin C and vitamin C plus E improve the immune function in the elderly, Experimental Gerontology, Volume 142.
(27) EFSA NDA Panel (EFSA Panel on Dietetic Products, Nutrition and Allergies). Scientific Opinion on Dietary Reference Values for vitamin C. EFSA Journal. 2013;11(11):3418, 68 pp.
(28) Bonnefont-Rousselot D, Bonnel S, Borel P, Bouglé D, Cals M-J, Carbonneau M-A, et al. 2007. Cahier de formation en biologie médicale N°38 : Les Vitamines . Bioforma, formation continue des biologistes.
(29) Goetzl EJ, Wasserman SI, Gigli I, Austen KF. 1974. Amélioration de la migration aléatoire et de la réponse chimiotactique des leucocytes humains par l'acide ascorbique. J Clin Invest ; 53 (3): 813-818
(30) R Anderson, R Oosthuizen, R Maritz, A Theron, A J Van Rensburg. 1980. The effects of increasing weekly doses of ascorbate on certain cellular and humoral immune functions in normal volunteers, The American Journal of Clinical Nutrition, Volume 33, Issue 1, Pages 71–76,
(31) Hume R, Weyers E. 1973. Modifications de l'acide ascorbique leucocytaire pendant le rhume. Journal médical écossais ; 18 (1): 3-7
(32) Lauer A, -C, Groth N, Haag S, F, Darvin M, E, Lademann J, Meinke M. 2013. C: Dose-Dependent Vitamin C Uptake and Radical Scavenging Activity in Human Skin Measured with in vivo Electron Paramagnetic Resonance Spectroscopy. Skin Pharmacol Physiol ; 26:147-154
(33) Davis et al. 2016. Liposomal-encapsulated Ascorbic Acid: Influence on Vitamin C bioavailability and capacity to Protect against ischemia–reperfusion injury. Nutrition and Metabolic Insights ; 9 25–30.
(34) Corey J. Huck, Carol S. Johnston, Bonnie L. Beezhold, Pamela D. Swan. 2013. Vitamin C status and perception of effort during exercise in obese adults adhering to a calorie-reduced diet, Nutrition, Volume 29, Issue 1, Pages 42-45.
(35) Richard Colombo. 2001. Etude de la carence en vitamine C dans une population gériatrique hospitalisée. Sciences du Vivant.
(36) Ratsimamanga, A. 1939. INFLUENCE DE L'A. ASCORBIQUE SUR LE COMPORTEMENT DE L'ORGANISME AU REPOS. Le Travail Humain, 7(3), 303-321.
(37) Braulio Gomez Ruiz. Prédiction de la dégradation de la vitamine C en conditions de traitement thermique : étude en milieu modèle liquide entre 50 et 90 °C. Chimie analytique. AgroParisTech, 2016. Français.23 CONFIDENTIEL
(38) ANSM. 2017. Résumé des caractéristiques du produit, REVITALOSE.
(39) Doutre S. 2009. Le système immunitaire cutané. Service Dermatologie du CHU de Bordeaux. EM consulte.
(40) Renaud. 2003. Fer, vitamine C et acide folique : convergence sanguine, Journal de Pédiatrie et de Puériculture. Volume 16, Issue 5, p.281-283.
(41) J. D. Cook, E. R. Monsen, 1977. Vitamin C, the common cold, and iron absorption, The American Journal of Clinical Nutrition, Volume 30, Issue 2, p.235–241.
(42) Université médicale virtuelle Francophone. 2011. Le Fer. Collège des enseignants de Nutrition, p.3-10.
(43) Marc P. McRae. 2006. The efficacy of vitamin C supplementation on reducing total serum cholesterol in human subjects: a review and analysis of 51 experimental trials. Journal of Chiropractic Medicine, Volume 5, Issue 1, p.2-12,
(44) Nutripure. 2020. Complément Mutlivitamines.
Composition Gélule
Ingrédients : Acide L-ascorbique Quali®-C (Vitamine C), gélule d’origine végétale (agent d’enrobage : pullulan), citrate de calcium, huile de tournesol (0.7%).
Composition Poudre
Ingrédient : Acide L-ascorbique (vitamine C) Quali®-C (Origine UE).
Quali®-C est une marque déposée de DSM Nutritional Products.
Indications
Complément alimentaire à base de vitamine C.
Informations Nutritionnelles
Version gélules
| Informations nutritionnelles | Quantité par dose journalière (1 gélule) | % AJR |
|---|---|---|
| Vitamine C | 750mg | 938 |
Version poudre
| Informations nutritionnelles | Quantité par dose journalière (2 dosettes) | % AJR |
|---|---|---|
| Vitamine C | 1000mg | 1250 |
*Valeurs indicatives
Transparence
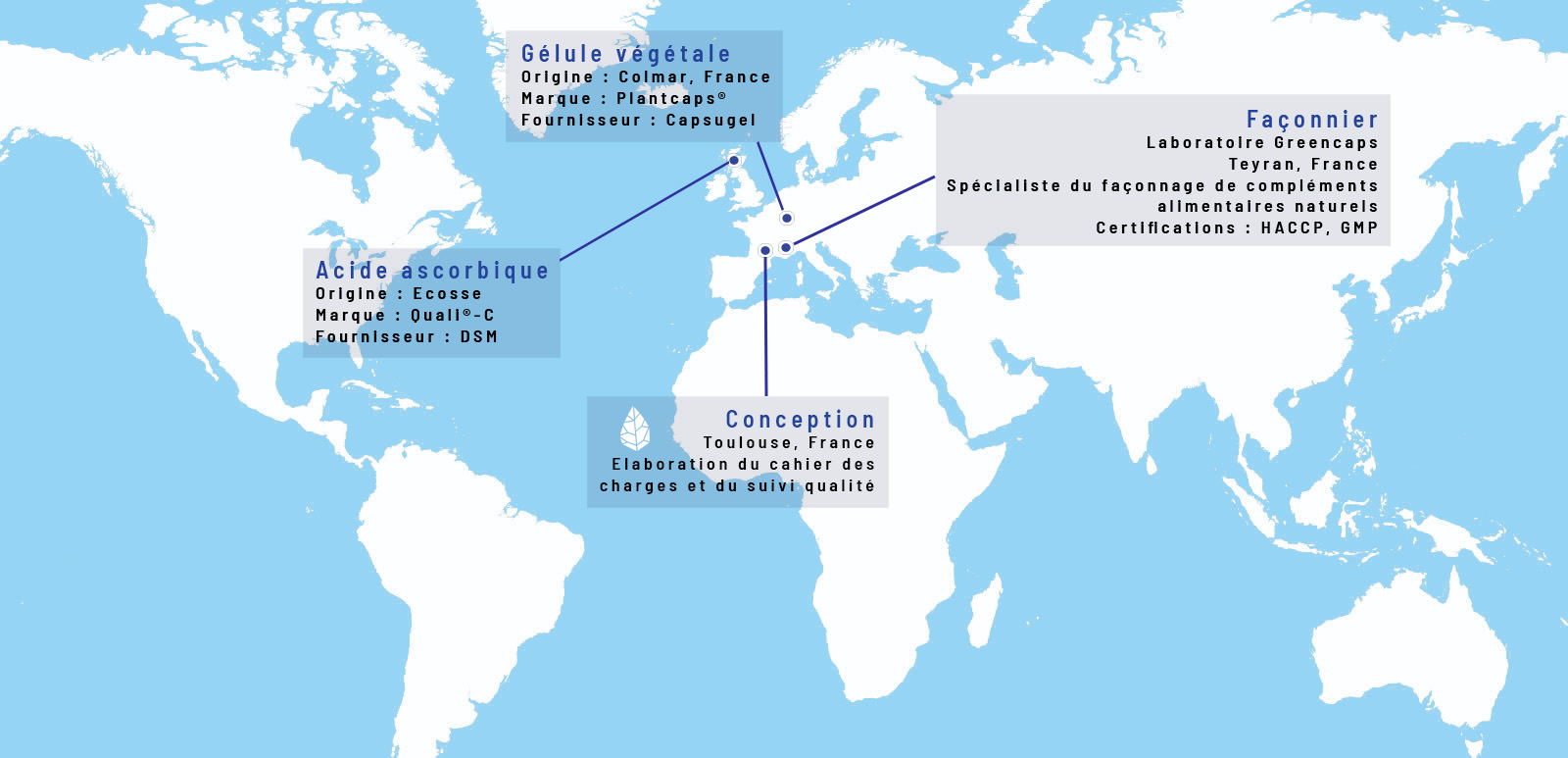
Avertissement
Les compléments alimentaires doivent être utilisés dans le cadre d’un mode de vie sain et ne pas être utilisés comme substituts d’un régime alimentaire varié et équilibré. Ne pas dépasser la dose journalière recommandée. Tenir hors de portée des enfants. Réservé à l'adulte. Les femmes enceintes et allaitantes sont invitées à prendre l’attache d’un professionnel de santé avant toute supplémentation. Les personnes ayant des problèmes rénaux ne doivent pas consommer plus de grandes quantité de vitamine C par jour en raison, entre autres, du risque d'hyperoxalémie. Privilégier dans ce cas le Multivitamines. Une consommation excessive journalière peut avoir des effets laxatifs.
Dosage & Préparation
![]() Version gélule : Prendre 1 gélule par jour avec un verre d’eau, de préférence le matin.
Version gélule : Prendre 1 gélule par jour avec un verre d’eau, de préférence le matin.
![]() Version poudre : Prendre 1g (2 dosettes) par jour avec un verre d’eau, de préférence le matin. Cuillère doseuse incluse.
Version poudre : Prendre 1g (2 dosettes) par jour avec un verre d’eau, de préférence le matin. Cuillère doseuse incluse.
Non, l'excès de vitamine C n'est pas dangereux pour la santé. Vous pourrez ressentir quelques effets indésirables comme des troubles digestifs, des maux de tête ou des insomnies mais rien de grave.
La quantité de vitamine C à consommer par jour est de 100mg sachant que vous pouvez aller jusqu'à 1000mg par jour en vitamine C sans risques d'effets indésirables sur votre santé.
La vitamine C se trouve principalment dans les fruits et les légumes. Pour faire le plein de vitamine C, n'hésitez pas à manger 5 fruits et légumes par jour comme le conseillent les docteurs.
Les signes d'un manque de vitamine C peuvent être : perte d'appétit, fatigue physique, maux de tête et système immunitaire plus faible = vous tombez souvent malade.
La vitamine C a de nombreux bienfaits sur la santé. Tout d'abord, la vitamine C lutte contre le stress oxydatif puisqu'elle permet d'augmenter le nombre d'antioxydants dans l'organisme.La vitamine C contribue au fonctionnement normal du système immunitaire. La vitamine C diminue la fatigue grâce à son action sur le fer. En effet, la vitamine C améliore l'absorption du fer dans votre organisme. L'oxygène circule mieux, vous êtes donc moins fatigué ! Enfin, la vitamine C baisse le taux de cholestérol !
Les fruits et les légumes sont les aliments contenant le plus de vitamine C naturellement. Le top 3 des fruits contenant de la vitamine C sont la cerise d'acérola, la goyave et le jujube séché (datte chinoise). Le top 3 des légumes contenant de la vitamine C sont la ciboulette séchée, le piment vert et le poivron.